Muchas veces, al hablar de coche eléctrico, acaba por salir el ‘coche de hidrógeno’ o incluso la ‘tecnología del hidrógeno’, ‘cultura del hidrógeno’ o la ‘cultura del hidrógeno’. Pero ¿Qué significa esta expresión? [1].
Como ya se ha dicho antes, el hidrógeno es un elemento bastante particular. Lo suficiente como para que no se tenga nada claro dónde ubicarlo en la tabla periódica. Al fin y al cabo, es el elemento más sencillo (y abundante!) de todos, al constar básicamente de un electrón y de un protón. Además es un átomo que es tan feliz de acoger otro electrón bajo su ala como de compartir el suyo, o de convertirse en un protón solitario.
Por eso es el elemento clave de un tipo de reacciones químicas conocidas como ‘de intercambio de protones’, más comúnmente llamadas ácidos y bases [2]. Pero eso no quita que además también sea un elemento usado en las reacciones redox que antes se han comentado como base de las baterías.
Dado que es un elemento muy ligero, pequeño, y abundante, es extremadamente interesante su uso para reacciones energéticas. Si tenemos en cuenta que la reacción química más violenta que existe, y por tanto, la que más energía da, es la que combina el hidrógeno con el oxígeno, dando lugar a agua. (Hidrogeno significa ‘generador de agua’).
Todo esto combinado significa que la mayor densidad de energía que podemos encontrar en una reacción química se corresponde con el hidrógeno. De hecho, los hidrocarburos (derivados del petróleo y del gas) son combinaciones de hidrógeno y carbono (la base de la química orgánica), y cuanto mayor contenido en hidrógeno, más ligeros, y también más energéticos.
Un Kg de H2, al reaccionar completamente con el oxígeno, desprende una energía de 39.9 KWh, lo cual es mucho, y encima, violentamente.
Así pues, se puede usar de dos maneras: quemándolo, o, dado que el credo actual de nuestra sociedad prefiere la aséptica electricidad, bien mediante celdas de combustible o pilas de combustible, que es un tipo de batería o pila eléctrica un poco particular.
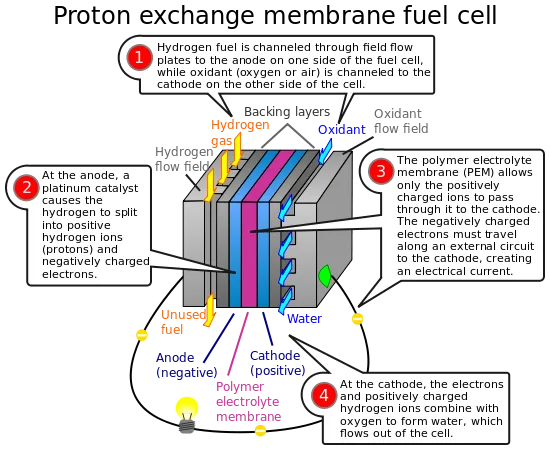
Las celdas de combustible en el fondo son como baterías [3]. Utilizan la oxidación de un elemento (el hidrógeno en casi todos los casos, aunque hay de metanol o de metano) de forma controlada, mediante la circulación de los electrones de un polo al otro. La diferencia entre éstas y las baterías es que las primeras tienen al oxidante (el oxígeno) y al elemento a oxidar (el hidrógeno) externas al sistema, mientras que las segundas lo tienen dentro de sí mismas.
Esto hace que las celdas de combustible sean interesantes: el hidrógeno se puede almacenar separadamente, en un tanque a presión, y por tanto, rellenar rápidamente, mientras que el oxígeno es aún mejor: lo cogemos de la atmósfera con lo que no tenemos que cargar con él. Encima, con lo liviano que es el hidrógeno, poco peso más vamos a cargar, haciendo, en un principio, todo el sistema más liviano y sencillo.
Ideal idealísimo, idealizado hasta el paroxismo.
Éstas son las ventajas. Las que nos cuentan. Lo único que promulgan a bombo y platillo los adalides de esta tecnología. Y como siempre, lo que interesa está en lo que se calla.
Veamos. Hay varias cosas que comentar, y dado que en el tema que nos ocupa hay interés en las celdas de combustible, vamos a hablar de la aplicación en coches eléctricos.
Porque en realidad, un ‘coche de hidrógeno’ es un coche eléctrico híbrido serie. Es decir, tiene un motor eléctrico que es alimentado a partir de una batería, y ésta es recargada a partir de una celda de combustible que genera la electricidad a partir de hidrógeno almacenado en alguna parte, y oxígeno, a veces, también almacenado dentro del mismo vehículo.
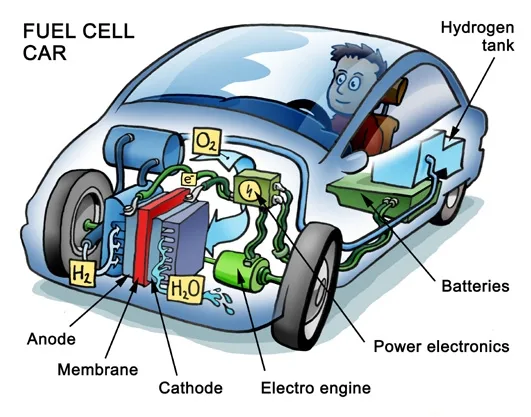
Empezando por lo más nimio, la celda de combustible es un elemento un poco particular que no admite grandes rangos de variación del punto de trabajo. Es decir, si la celda tiene una potencia nominal de 100KW, el rango habitual de trabajo será entre 20 – 30 KW de mínimo, hasta los 100KW de máximo, siendo ideal mantenerla entorno a los 70 KW, dependiendo mucho del modelo. Y encima, la variación no puede ser rápida. Al menos, no cómo es necesario en un coche, con acelerones y frenazos.
Encima, no es fácilmente reversible por motivos que veremos más adelante, aunque en un principio aceptaría tal función.
Por todo esto, es necesario el poner una batería, para soportar las variaciones de demanda y las recargas por frenado regenerativo, o mejor, supercodensadores, tal y cómo se comento en la entrada anterior. Así pues, no se trata de ahorrarse la batería, se trata de reducir sus dimensiones o sustituirla por algo que tenga la capacidad de potencia necesaria para trabajar a corto plazo, mientras la celda de combustible proporciona básicamente la autonomía.
Uno de los motivos por los que las celdas de combustible no pueden trabajar fuera de ciertos rangos es básicamente debido a que la membrana semipermeable, que hace las veces del electrolito de una batería, necesita un cierto grado de humedad para trabajar. Poca potencia significa poca conversión de H2 + O2 a agua, y por tanto, poca humedad. Un exceso de potencia, y la cantidad de H2 que puede pasar limita la misma, con la consecuente caída de rendimiento, además de tener más agua en la salida, lo cual reduce la cantidad de oxígeno para la reacción.
Además, el factor limitante es la cantidad de O2 que tiene para reaccionar. Si hacemos circular aire, el O2 sólo representa alrededor de una quinta parte del volumen de gas circulando por el otro lado de la membrana. Si queremos que el sistema sea de escasas dimensiones y peso, hay que hacer que el O2 tenga mayor presencia, así que o bien se comprime el aire (con la consecuente pérdida de energía en el proceso), o bien se usa O2 puro almacenado en alguna parte. De esta manera, se obtienen mejores rendimientos y respuestas más rápidas.
Otras dos particularidades de las celdas de combustible de baja temperatura son su catalizador (platino) [4] y la vida útil de la membrana semipermeable [5]. Ambos son críticos y muy sensibles a impurezas, además de caros. Lo cual hace que un hidrógeno contaminado, pongamos, con metano, estropee tanto uno como la otra, con la consecuente pérdida de rendimiento. Esto provoca que la vida de las membranas semipermeables sea limitada, unos 2 años.
Por supuesto, el platino es mucho más caro que dichas membranas, pero al menos dura lo mismo que la celda de combustible. Y no se utiliza poco: cada celda genera alrededor de 1V o algo menos de tensión, lo cual obliga a poner varios cientos en serie, junto con las canalizaciones de gases y líquidos (agua de escape), lo cual genera un volumen y peso considerables, aunque mucho menores que para una batería.
El problema gordo de verdad con el hidrógeno para cualquier uso similar, aunque sea combustión, es el almacenamiento del mismo. Se trata de un elemento muy volátil, con el punto de fusión (es decir, al temperatura a la cual pasa de sólido a líquido) de 2ºK, o sea, -259.14ºC. Un poco frío. La temperatura de evaporación, es decir, el paso de líquido a gas, es mayor. 252.87º bajo cero. Así que en usos de automoción, se suele usar como gas.

Dado que el hidrógeno es bastante ligero. Muy ligero, de hecho, como gas ocupa mucho sitio. Tanto es así que se usaba como elemento ‘flotador’ para los dirigibles como el Hindemburg [6]. En las llamadas Condiciones Normales (0ºC, 1 atmósfera de presión), el un mol de hidrógeno, es decir, 2g de dicho gas, ocupan la friolera de 22,4 litros de aire. Un kilo, ocupa 11,2 metros cúbicos, lo mismo que un coche. Y son ‘sólo’ unos 40KWh.
Dado que el volumen sube con la temperatura, y la temperatura ambiente confortable está algo por encima de 0ºC, la única salida es comprimir el gas para que ocupe menos sitio. Las presiones entonces se convierten en algo importante: más presión, más pequeño el depósito, quizás más ligero, aunque también tiene que ser más robusto.
Si encima tenemos en cuenta que el hidrógeno, al ser tan pequeño, atraviesa fácilmente las paredes de los depósitos, resulta que hace falta hacer éstos compactos, a la vez que no conviene subir mucho la presión. Por tanto, almacenarlo no es tan sencillo como se puede preveer.
El depósito del Honda FCX [7] tiene una capacidad para 4,1 Kg de hidrógeno, ocupa 180 litros de maletero (lo cual no es tanto), y pesa 91Kg. Mejor que cualquier batería en este aspecto, pero es que tampoco se libra de la batería, y dicho depósito ocupa y pesa mucho más que un depósito de combustibles líquidos. Y aún así, tiene pérdidas elevadas.
Lo normal en una instalación de almacenamiento de H2 es una pérdida del orden del 2% diario en un depósito lleno a tope de presión. Menor presión significa menores pérdidas, pero también menos gas almacenado.
A todo esto, hay que añadir algunos puntos de consideración. El primero es que el hidrógeno es un gas incoloro, inodoro e insípido, como el agua, pero en gas. Es volátil, ligero, se mezcla muy bien con cualquier otro gas. Y sobre todo, es inflamable.
Muy inflamable.
Explosivo, de hecho. Y la llama además es prácticamente invisible, poco luminosa.
De hecho, es tan energético que es el mejor combustible para cohetes que existe. La gente que trabaja en la NASA [8], es decir, una banda de aficionados, lo utiliza en los cohetes con mejores prestaciones, en los realmente ‘especiales’. Para los normales, como el Apolo [9], utiliza combustibles líquidos a base de hidrocarburos.

Es curioso que estos señores de la NASA eviten lo que pueden el uso del hidrógeno. No será por falta de tecnología ni financiación ni capacidad. Se trata más bien de una cuestión de seguridad y almacenamiento (y la seguridad del mismo). Un depósito de H2 para cohete ocupa mucho sitio, y por tanto es pesado, y además, necesita un buen aislamiento térmico y sistemas de contención internos para que el hidrógeno líquido no vaya salpicando y meneándose por todas partes, desestabilizando el cohete.
Además, trabajan con hidrógeno líquido (para reducir presión y pérdidas), lo cual es fuertemente frío, criogénico, y como tal, se usan para enfriar los motores de los cohetes. Los metales y elementos utilizados a tales temperaturas deben ser de ciertos materiales, pues muchos se vuelven muy quebradizos y frágiles en semejantes condiciones. Lo cual es propicio a los accidentes.
Respecto de su uso en otros campos, como los dirigibles, creo que basta recordar cómo acabo el dirigible Hindemburg. Aunque los cazadores de mitos afirman que lo que ardió fue la cubierta por el ‘fuego termita’, lo cierto es que el fuego del hidrógeno es prácticamente invisible, y el brillo del fuego termita lo hubiese enmascarado totalmente, además de acelerarse enormemente
Por si el almacenamiento de hidrógeno no asusta directamente, hay otro elemento desconocido sobre el mismo que hace que la gente considere mal sus ventajas. Ni asusta (directamente) ni preocupa en exceso, pero al menos queda claro que las cosas no son lo que parece.
Se trata de que el mismo NO se encuentra libre en la naturaleza. Es abundante, pero siempre está enlazado químicamente con otros elementos, con diferencia, el oxígeno, en forma de agua, pero seguido por otros elementos de sobras conocidos: los hidrocarburos y la química orgánica en general.
Mientras el discurso popular dice que el hidrógeno es abundante y sólo se convierte en agua al usarlo para obtener energía, casi nadie dice nada de cómo se obtiene el mismo del medio ambiente. Algunos se atreven a decir que por electrólisis, que uno se pone la celda de combustible en casa, le mete electricidad, y saca hidrógeno. Lo cual es bastante correcto, pero inexacto.
La triste realidad es que más del 95% del hidrógeno que se usa industrialmente, se obtiene de hidrocarburos, y sólo una ínfima parte, de agua [10]. Directamente, en la reacción química más favorable, del metano se obtiene 1Kg de H2 para echar a la atmósfera 12Kg de CO2. Sin contar lo que se echa para obtener la energía necesaria para el proceso, ni las externalidades de tener que comprimir el H2 para su almacenamiento y transporte.
‘Afortunadamente’, la gran mayoría de H2 se usa tal y como se produce, para obtener otros elementos importantes: nitratos para uso industrial, o, mayormente, agrícola [11]. Y para eso, se utiliza entre el 2 y el 3% del gas natural que se extrae del subsuelo, más una parte importante de petróleo, en la producción y la energía necesaria para dicho proceso.
Así pues, utilizar hidrógeno es lo mismo que utilizar gas natural, pero de una manera menos eficiente. No se emite CO2 en el vehículo, pero se desplaza su emisión hacia las plantas de generación del hidrógeno, sin contar toda la cadena de distribución y almacenamiento.
La presunción de utilizar una celda de combustible en funcionamiento inverso, o, directamente, hidrólisis con electricidad en casa no es descabellada, ni precisamente, incorrecta. Además, sería una manera de almacenar energía excedente de producción en el momento en que ésta se genera, si no se puede usar, lo cual es precisamente el punto fuerte de este tipo de solución, el valor añadido, la razón básica para desplazarse hacia este tipo de energía.
Sin embargo, hay que contar con la compresión añadida para almacenar dicho hidrógeno. Además de los depósitos, cuyo peso y volumen no son tan importantes en una vivienda como en un vehículo, el equipo de presión consume energía, y ésta difícilmente puede ser reciclada. Y este equipo también pesa, ocupa espacio, lo cual es precisamente el motivo por el cual en las frenadas regenerativas no se puede utilizar la celda de combustible del vehículo para obtener hidrógeno.
Pero el principal inconveniente del sistema, además de la corta vida, complejidad, pesos, volúmenes, pérdidas, peligros, es su escasísimo rendimiento. Además de ser sólo un vector energético, no energía directamente concentrada como el caso del petróleo, gas o carbón.
Veamos el concepto de vector energético [12]:
Energía eléctrica Proceso Almacenamiento Proceso Energía eléctrica.
Si los procesos se llaman carga/descarga o electrólisis/oxidación controlada, y el almacenamiento se llama Batería o Depósito de Hidrógeno, es secundario. El concepto es el mismo: a partir de energía eléctrica en ciertas condiciones, almacenada mediante algunos sistemas y procesos, obtenemos energía eléctrica en otro momento y lugar, en otras condiciones.
Éste es el principio de vector energético: un sistema de transformación y almacenamiento de energía. Lo mismo da que sea por batería que sea por hidrógeno o algún otro elemento, como biocombustibles.
Lo que importa, es la energía que entra, y la energía que sale. Para el caso se trata, directamente, de energía eléctrica en la entrada, que puede ser, por ejemplo, obtenida a partir de fotovoltaica y/o eólica u otro tipo de renovable, mejor si es intermitente, pues así se puede aprovechar mejor (más sobre este importante punto en la última entrega), para luego utilizar dicha energía, también de tipo eléctrico, bajo la demanda de algún usuario (por ejemplo, el pedal del acelerador).
Por la termodinámica, nunca obtendremos tanta energía a la salida como la que le hemos metido en la entrada. Es decir, que por cada KWh que le metamos al sistema, sólo recuperaremos una parte, menos del KWh que le hemos metido. Esto, que en realidad es una TRE inferior a uno, sólo tiene sentido, y mucho, para casos en los que la energía se obtiene de manera intermitente y necesita ser usada a discreción. En tal caso, como cualquier TRE, interesa que sea lo más alta posible.
Y aquí es donde ‘muere’ el hidrógeno. El principal motivo es el engorro y consumo de la compresión y almacenamiento (sin contar las pérdidas de los depósitos), pero los rendimientos tanto de la electrólisis, como de la celda de combustible, dejan mucho que desear.
Aunque en el aspecto de rendimiento se va a entrar en detalle en otra entrada posterior, al menos en este caso se va a hacer un escueto recuento del rendimiento de uno coche de celda de combustible como el Honda FCX, con un eléctrico puro, como por ejemplo, el Renault Fluence.
El Honda FCX consume alrededor de 1Kg de H2 por cada 100 Km. Lo cual equivale a unos 40KWh. El Renault Fluence, alrededor de 16KWh. Valores nominales del fabricante en ambos casos. Y lo peor, es que las pérdidas para obtener el hidrógeno y comprimirlo es donde está la mayoría de la pérdida de rendimiento.
De hecho, haciendo los números redondos, estaríamos hablando de un rendimiento entre la electricidad que sale por la que entra de alrededor del 30 – 35% para el FCX (como un diesel!!), con alrededor del 60 – 70% del Fluence, contando de KWh en el enchufe a Km realizados. Directamente el doble. Y eso que el hidrógeno, en teoría, permite un coche más ligero y con menos espacio para el sistema de energía. La única ventaja real es la recarga del depósito de H2, que es rápida.
La hidrólisis, en condiciones reales de la industria, difícilmente supera el 60%, aunque hay algunos casos que llega al 70%, si bien en muchos otros está en el 50%. Eso implica un gran gasto de electricidad para conseguir el hidrógeno, y por tanto, encarece el mismo. Si con una pequeña fracción del coste, se obtiene hidrógeno a partir del gas natural, que es exactamente la situación en 2014, y no parece que vaya a mejorar, especialmente en unos EEUU con el gas a precios irrisorios debido al frácking [13], es lógico que el hidrógeno no tenga un origen ‘renovable’.
Además, es una tecnología, que aunque lleve bastante tiempo en desarrollo, todavía no está, ni de lejos, madura. Lo bueno es que podría ser que hubiese mejoras sustanciales, aunque lo malo es que apenas se espera que lleguen al nivel al que están actualmente las baterías a nivel de rendimientos, coste, vida útil, sencillez, infraestructura, inversión, estado de la tecnología, situación del automóvil y obtención, en general, del hidrógeno mismo. El cambio a una ‘economía del hidrógeno’ no sería realmente rápido, corto ni sencillo.

Curiosamente, precisamente Opel considera que las baterías son sólo un paso intermedio hacia el ‘Wasserstoff’.
[1] http://en.wikipedia.org/wiki/Hydrogen_economy
[2] http://es.wikipedia.org/wiki/Reacci%C3%B3n_%C3%A1cido-base
[3] http://en.wikipedia.org/wiki/Fuel_cell
[4] http://en.wikipedia.org/wiki/Plantinum
[5] http://en.wikipedia.org/wiki/Polymer_electrolyte_membrane
[6] http://en.wikipedia.org/wiki/LZ_129_Hindenburg
[7] http://es.wikipedia.org/wiki/Honda_FCX_Clarity
[8] http://en.wikipedia.org/wiki/Space_Shuttle_Main_Engines
[9] http://en.wikipedia.org/wiki/Saturn_V
[10] http://www.aecientificos.es/empresas/aecientificos/documentos/LAECONOMIADELHIDROGENO.pdf
[11] http://en.wikipedia.org/wiki/Haber_process
[12] http://en.wikipedia.org/wiki/Energy_carrier
[13] http://crashoil.blogspot.com.es/2013/11/el-fracking-se-fractura.html





